��ܰ��ʾ���ֻ��û������·���ԭ��ҳ�����桱���в鿴���ģ�Ч����ѣ�
16. ����A—D���飬ÿ����������Ӧ������������Ӧ����ͬһ���ӷ���ʽ��ʾ���ǣ�
|
|
���� |
���� |
|
A |
����H2SO4����Ba(OH)2��Һ�� |
����NaHSO4����Ba(OH)2��Һ�� |
|
B |
����NaOH����Al2(SO4)3��Һ�� |
����Al2(SO4)3��Һ���백ˮ�� |
|
C |
FeO������������ |
FeO��������ϡ���� |
|
D |
0.1 mol Cl2ͨ�뺬0.2 mol FeBr2����Һ�� |
0.1 mol Cl2ͨ�뺬0.2 mol FeCl2����Һ�� |
17.
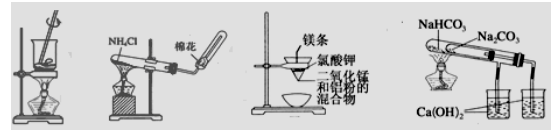
������װ���ܴﵽ�й�ʵ��Ŀ�ĵ���
�� �� �� ��
A���ü�ͼװ�����պ����ɺ����� B������ͼװ��ʵ�����ư���
C���ñ�ͼװ�ÿ��Ƶý����� D���ö�ͼװ����֤NaHCO
3��Na
2CO
3���ȶ���
18. ��3�ݵ�������С�մ�1��ֱ��������ǡ����ȫ��Ӧ����2�����ȼ��ȣ�ʹ�䲿�ַֽ����������ǡ����ȫ��Ӧ����3�����ȼ��ȣ�ʹ����ȫ�ֽ����������ǡ����ȫ��Ӧ��������������ʵ���Ũ����ͬ���������������ֱ�ΪV
1��V
2��V
3����V
1��V
2��V
3�Ĵ�С��ϵ��ȷ����
A��V
1>V
2>V
3 B��V
1>V
3>V
2 C��V
2>V
3>V
1 D��V
1��V
2��V
3
19. ij��ȤС��̽��SO
2���廹ԭFe
3��������ʹ�õ�ҩƷ��װ������ͼ��ʾ������˵������������
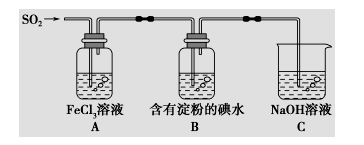
A���ܱ���I
���Ļ�ԭ������SO
2��������B����ɫ��Һ��ɫ
B��װ��C������������SO
2β������ֹ��Ⱦ����
C��Ϊ����֤A�з�����������ԭ��Ӧ��������ϡ�����ữ��BaCl
2��Һ��������ɫ����
D��Ϊ����֤A�з�����������ԭ��Ӧ������KMnO
4��Һ���Ϻ�ɫ��ȥ
20. FeS��һ��Ũ�ȵ�HNO
3��Ӧ������Fe(NO
3)
3��Fe
2(SO
4)
3��NO
2��N
2O
4��NO��H
2O����NO
2��N
2O
4��NO�����ʵ���֮��Ϊ1�U1�U1ʱ��ʵ�ʲμӷ�Ӧ��FeS��HNO
3�����ʵ���֮��Ϊ�� ��
A��1:6 B��1:7 C��2:11 D��16:25
21. (12��)���ٶ�����̼���ŷ���һ����Ҫ���⡣
(1)CO
2��������ɺϳɵ�̼ϩ����2CO
2(g)+6H
2(g)

C
2H
4(g)+4H
2O(g) ��H
��0.1 MPaʱ����

��1��3Ͷ�ϣ�ͼ14��ʾ��ͬ�¶�(T)�£�ƽ��ʱ��������̬���ʵ����ʵ���(n)�Ĺ�ϵ��
�ٸ÷�Ӧ�ġ�H__________0(��“>”��“��”��“<”)��
������b��ʾ������Ϊ__________��
�����CO
2��ƽ��ת���ʣ����ı��¶��⣬���ɲ�ȡ�Ĵ�ʩ��__________��
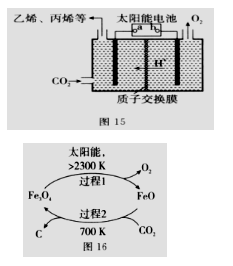
(2)��ǿ���Եĵ����ˮ��Һ�У����Բ������缫�����CO
2�ɵõ�����ȼ�ϣ���ԭ����ͼ15��ʾ��
�ٸù���������ת����ʽ��Ҫ��_________��
��bΪ��Դ��________(��“��”��“��”)�������ʱ��������ϩ�ĵ缫��Ӧʽ��_________��
(3)��CO
2Ϊԭ����ȡ̼(C)��̫���ܹ�����ͼ16��ʾ��
�ٹ���1ÿ��Ӧ1mol Fe
3O
4ת�Ƶ��ӵ����ʵ���Ϊ__________��
�ڹ���2������Ӧ�Ļ�ѧ����ʽ��__________��
22. (12��)ij����������ɰ�����в����Ĺ�����ϣ���Ҫ����MgCO
3��MgSiO
3�� CaMg(CO
3)
2��Al
2O
3��Fe
2O
3�ȣ���������þ�Ĺ����������£�
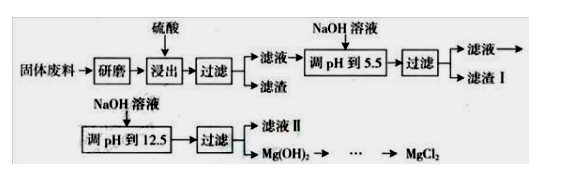
����������������������ʽ��ȫ����ʱ��Һ��pH���±�����ش��������⣺
|
������ |
Fe3+ |
Al3+ |
Mg2+ |
|
PH |
3.2 |
5.2 |
12.4 |
(1)“����”�����У�Ϊ���þ�Ľ����ʣ��ɲ�ȡ�Ĵ�ʩ�� (Ҫ��д������)��
(2)����I����Ҫ�ɷ��� ��
(3)����Һ���пɻ������õ���Ҫ������ ��
(4)����MgCl
2��Һ�������ɵõ��Ĺ�����____����Ҫ�õ�MgCl
2Ӧ��ȡ�IJ�����_____��
(5)��ϡ�������ʱ�γ����������ӷ���ʽ��_____________________________��
23. (10��)�Ͼ���ʾ�������к�SiO
2��Fe
2O
3��CeO
2��FeO�����ʡ�ij����С���Դ˲�����ĩΪԭ�ϣ��Ƶ�Ce(OH)
4��������立���Fe
2(SO
4)
3·(NH
4)
2SO
4·24H
2O�ݣ�����������£�
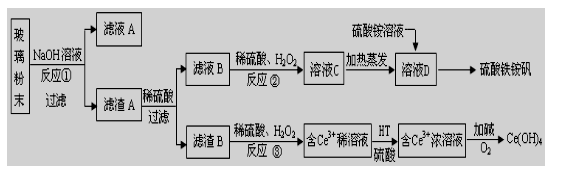
��֪�������������£�����ˮ��Һ����Ce
3+��Ce
4+������Ҫ������ʽ��Ce
4+�н�ǿ�����ԣ���CeO
2������ϡ���ᣬҲ������NaOH��Һ��
�ش��������⣺
(1)��Ӧ�ٵ����ӷ���ʽ�� ������
(2)��Ӧ����H
2O
2�������� ��
(3)��Ӧ�۵����ӷ���ʽ�� �� ����
(4)��֪�л���HT�ܽ�Ce
3+��ˮ��Һ����ȡ�������ù��̿ɱ�ʾΪ��
2Ce
3+ (ˮ��)+ 6HT(�л���) 2CeT
3 (���)+ 6H
+(ˮ��)
��ƽ��ǶȽ��ͣ���CeT
3 (���)����H
2SO
4 ��ýϴ��ĺ�Ce
3+��ˮ��Һ��ԭ���� ��
(5)������立���Fe
2(SO
4)
3·(NH
4)
2SO
4·24H
2O�ݹ㷺����ˮ�ľ����������侻ˮԭ�������ӷ���ʽ������ ��
24. (13��)ʵ��С��ͬѧ����һ����ij��ֽ���۳���Ư��Һ(NaCl��NaClO�Ļ��Һ)����ʢ�ű���KAl(SO
4)
2��Һ�ij��У�����ж��¼�����С��ͬѧΪ̽���ж�ԭ�����������ʵ�顣
(1)С��ͬѧ����Ư��Һ����Ư�������������Ʋ⣬Ư��Һ��ClO
�����������ԡ�ʵ�����£�
��. ��pH��ֽ���飬Ư��ҺpH>7������

��ҺpH<7��
��. ȡ10 mLƯ��Һ�����μ���Na
2SO
3��Һ��BaCl
2��Һ���а�ɫ�������ɣ��������ɫ�������������ᡣ
��. ��ȡ10 mL��Ư��Һ������Ʒ����Һ����Һ��ɫ��dz��һ��ʱ�����Ϊ��ɫ��
��. ��ȡ10 mLƯ��Һ������Ʒ����Һ����������ϡ�����ữ����Һ��ɫ������Ϊ��ɫ��
��Ư��ҺpH����7��ԭ����(�����ӷ���ʽ��ʾ)__________��
����ʵ���ó�ClO
�����������ԣ�д����Ӧ�����ӷ���ʽ__________��
�۶Ա�ʵ���͢�˵��ClO
������������Һ����ԵĹ�ϵ��__________��
(2)С��ͬѧ����(1)�е�ʵ�飬�����Ư��Һ��������Һ����Cl
2���ɡ�
��ͼ18��ʾ��װ�ü���ʵ�飬̽��Ư��Һ��������Һ���Ƿ��ܷ�Ӧ����Cl
2��
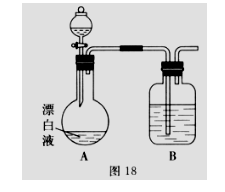
��װ��B��������__________��ʢ�ŵ�ҩƷ��__________��
������Һ©����������ƿ�м������ᣬ������ƿ���л���ɫ���������A�з�Ӧ�����ӷ���ʽ__________��
������Һ©����������ƿ�м��뱥��

��Һ���۲쵽���������İ�ɫ��״������ͬʱ�л���ɫ���������A�м�

��Һ��Ӧ�����ӷ���ʽ��__________��
(3)����ʵ��˵��Ư��Һ��������Һ��ϻ����Cl
2����ȡ10 mLƯ��Һ������BaCl
2��Һ��Ϻ���ͨ��SO
2����������ʵ������п��ܵ�ʵ��������__________��
25. (13��)������������Ҫ�ķ�������ij��ѧ��ȤС����̼��Ũ����Ϊ��ʼԭ�ϣ��������װ������һ��������������Ʒ�Ӧ�Ʊ��������ơ����г�װ�ú�A�м���װ�����ԣ��������Ѽ��飩���������ϣ���HNO
2Ϊ���ᣬ�����´��ڷ�Ӧ3HNO
2��HNO
3��2NO↑��H
2O��
����������Һ�У�NO
2���ɽ�MnO
4����ԭΪMn
2����
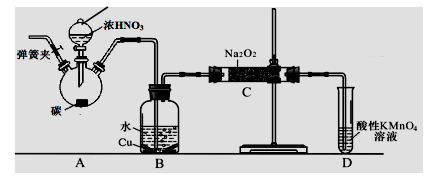
��NO����Ӧ���ɱ�����KMnO
4��Һ����Ϊ����
���л�ѧģ���� http://www.17xuexiba.com/hx/
 ������װ���ܴﵽ�й�ʵ��Ŀ�ĵ���
������װ���ܴﵽ�й�ʵ��Ŀ�ĵ���
 (2)��ǿ���Եĵ����ˮ��Һ�У����Բ������缫�����CO2�ɵõ�����ȼ�ϣ���ԭ����ͼ15��ʾ��
(2)��ǿ���Եĵ����ˮ��Һ�У����Բ������缫�����CO2�ɵõ�����ȼ�ϣ���ԭ����ͼ15��ʾ��


 ��NO����Ӧ���ɱ�����KMnO4��Һ����Ϊ����
��NO����Ӧ���ɱ�����KMnO4��Һ����Ϊ����